Несколько способов защиты файлов от чужого доступа
4-11-2014, 19:03 Безопасность
Рано или поздно, у каждого пользователя появляется потребность в разграничении прав доступа к определенным файлам и папкам на компьютере общесемейного или корпоративного назначения. Это могут быть родители, желающие оградить своих детей от воспроизведения изображений и видеоматериалов, содержащих элементы насилия, сцены эротического характера, аудиозаписией с использованием ненормативной лексики, а также люди, работающие с информацией, не подлежащей разглашению.
Самым верным решением в данной ситуации может оказаться создание учетных записей администратора и гостя, но для большинства пользователей такой способ может оказаться слишком сложным. Есть несколько более простых способов.
Первый способ по совместительству самый простой. Нужно всего лишь поместить файлы в архив и защитить его паролем.
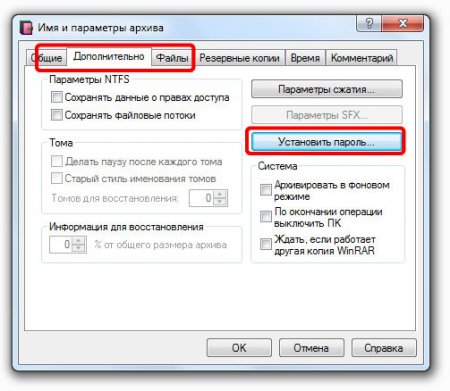
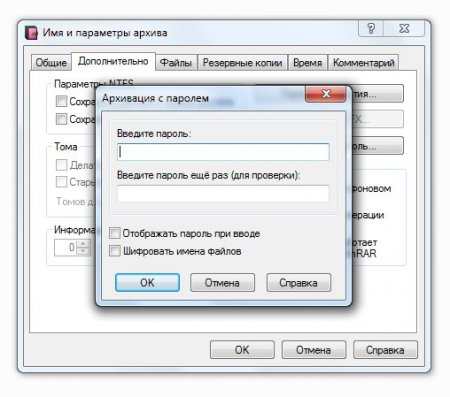
Но что делать, если под рукой нет архиватора?
Способ номер два предусматривает создание скрытой запароленной папки штатными средствами Windows 7.
Кроме обыкновенного блокнота Windows, вам больше ничего не потребуется.
Создайте новую папку и назовите её как угодно.
Создайте в папке новый текстовый документ, нажав правую кнопку мыши:
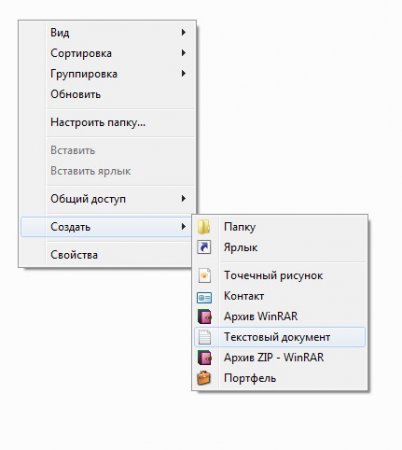
В файл скопируйте строки следующего содержания:
cls
@ECHO OFF
title Folder Private
if EXIST «Control Panel.{21EC2020-3AEA-1069-A2DD-08002B30309D}» goto UNLOCK
if NOT EXIST Private goto MDLOCKER
:CONFIRM
echo Are you sure you want to lock the folder(Y/N)
set/p «cho=>»
if %cho%==Y goto LOCK
if %cho%==y goto LOCK
if %cho%==n goto END
if %cho%==N goto END
echo Invalid choice.
goto CONFIRM
:LOCK
ren Private «Control Panel.{21EC2020-3AEA-1069-A2DD-08002B30309D}»
attrib +h +s «Control Panel.{21EC2020-3AEA-1069-A2DD-08002B30309D}»
echo Folder locked
goto End
:UNLOCK
echo Enter password to unlock folder
set/p «pass=>»
if NOT %pass%== ENTER YOUR PASSWORD HERE goto FAIL
attrib -h -s «Control Panel.{21EC2020-3AEA-1069-A2DD-08002B30309D}»
ren «Control Panel.{21EC2020-3AEA-1069-A2DD-08002B30309D}» Private
echo Folder Unlocked successfully
goto End
:FAIL
echo Invalid password
goto end
:MDLOCKER
md Private
echo Private created successfully
goto End
:End
Найдите в коде строки, содержащие текст: ENTER YOUR PASSWORD HERE:
Введите вместо этого текста свой пароль.
Зайдите в меню Файл > Сохранить как >
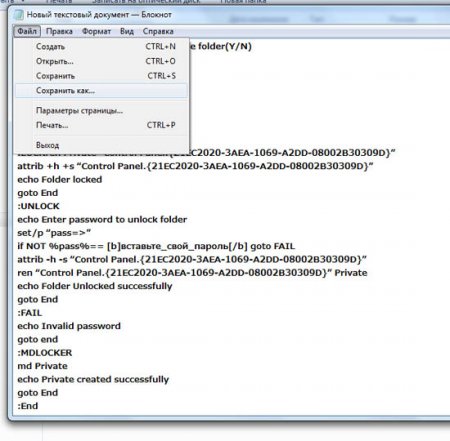
и в появившейся строке напишите: locker.bat. Нажмите кнопку сохранить.
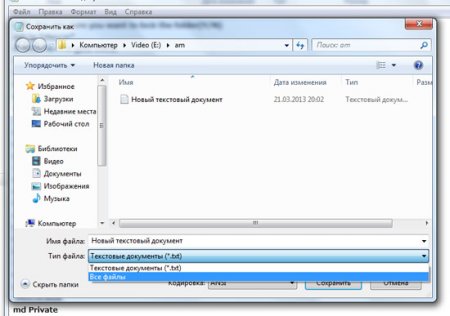
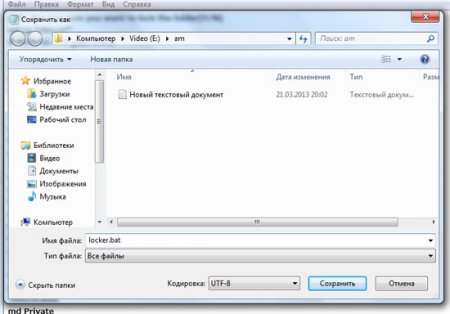
Вместо текстового документа у нас появится файл с именем locker. Запустите его.
Создастся папка под именем Private, в которую можно помещать файлы, содержание коих нужно скрыть от других пользователей.
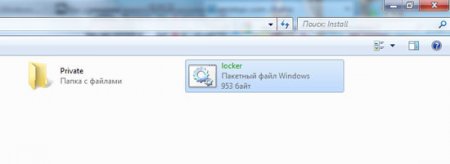
После копирования файлов запустите наш файл еще раз. На этот раз он выведет строку: Are you sure you want to lock the folder(Y/N):
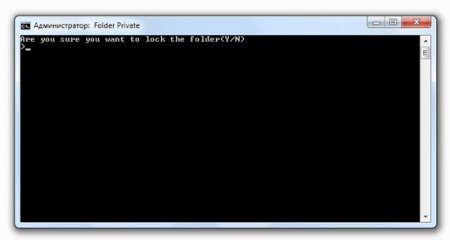
Нажимаем Y на клавиатуре и следом клавишу Enter.
Доступ к нашей папке будет заблокирован, а сама папка исчезнет.
Для доступа к папке запустите наш файл locker.bat и введите пароль.
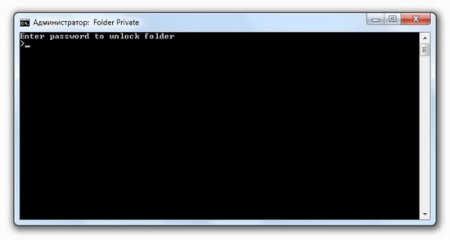
Снова появится папка, в которую можно добавлять файлы.
Такими простыми способами можно не только ограничивать доступ к папкам на домашнем компьютере, но и переносить их на рабочий компьютер, не боясь утечки конфеденциальной информации.
Наконец, третий способ подразумевает использование программы Folder GuardМатериалы по теме
 © Copyright 2024. Все права защищены.
© Copyright 2024. Все права защищены.